Zprávy CEM (SZÚ, Praha) 2007; 16(10-11): 493 – 497.
Tento článek je pokračováním první části, která byla otištěna v minulém čísle Zpráv CEM [4]
DIAGNOSTIKA – orientační přehled
Vzhledem k závažnosti a povaze onemocnění není sérologické vyšetření indikováno pouze klinickým podezřením, ale je rovněž součástí obligátních schémat (Zákon č. 258/00 Sb., vyhláška č.195/05 Sb.):
– u dárců krve, tkání a orgánů
– v rámci prenatální péče
– předoperační příprava
– při hospitalizaci.
– Rozsah povinného základního vyhledávacího vyšetření na příjici
základní screening novorozenců je specifikován ve vyhlášce č. 195/2005 Sb. § 7 odst. 2: … „Lékař dále provádí klinické a sérologické vyšetření na příjici s použitím jedné nespecifické a jedné specifické reakce u všech těhotných žen ve 3. a 7. měsíci těhotenství, i pupečníkové krve každého novorozence, u každé ženy před provedením interupce“. Nedodržení těchto norem může být následováno postihem.
Stejná vyhláška také upravuje náležitosti průvodního listu k vyšetření na infekční chorobu
v § 5 Zásady pro odběr a vyšetření biologického materiálu a náležitosti žádanky, odst. 3 Žádanka na vyšetření biologického materiálu musí obsahovat jméno, příjmení, rodné číslo a datum narození vyšetřované osoby, pokud nebylo rodné číslo přiděleno, adresu místa pobytu v ČR, …
Citované zákonné normy jsou obecně právně závazné a musí být dodrženy i v případě osob přicházejících k vyšetření na vlastní žádost.
1. PŘÍMÁ LABORATONÍ DIAGNOSTIKA
Detekce bakterie TPP v biologickém materiálu je vhodná prakticky pouze pro manifestní stadia, kdy je biologický materiál s treponematy přístupný odběru a kdy lze očekávat jejich přítomnost v dostatečném množství.Využití a standardizace přímých testů je však ovlivněno celou řadou podmínek, které mohou výrazně snížit citlivost vyšetření (lidský faktor, časová prodleva, náklady na provedení testu a jeho skutečný význam pro konkrétní stanovení diagnózy).
1.1. Zástinová mikroskopie – základní, standardní vyšetření při podezření na specifickou lézi na kůži nebo sliznici. Umožňuje vyšetřit serózní exsudát z lézí, liquor (CSF), amniovou tekutinu apod. Zpracování nativního preparátu vyžaduje zkušený personál. Identifikace bakterie spočívá v posouzení morfologie a motility (značné ovlivnění viskozitou prostředí a subjektivní chybou). Metoda není vhodná pro vyšetření tkání (z technických důvodů), vzorky odebrané z dutiny ústní mohou být falešně pozitivní, je možná záměna se zcela morfologicky shodnou, nepatogenní Treponema denticola .
1.2. Přímá imunofluorescence (DFA-TP) – klade sice stejné nároky na erudici personálu při odběru a zpracování vzorku, umožňuje však vyšetřovat fixovaný preparát (serózní exsudát z lézí, CSF, amniovou tekutinu, tkáně) s časovým odstupem v adekvátně vybavené laboratoři. Eliminuje také problém morfologické shody s nepatogenními treponematy z dutiny ústní. Nevýhodou jsou náklady na techniku (fluorescenční mikroskop) a nedostupnost komerčního diagnostika na našem trhu.
1.3. Impregnace kovy (stříbření) – původní histologická metodika je zdlouhavá a zatížená řadou artefaktů (změna morfologie mikrobů).
1.4. Inokulace zvířecímu hostiteli (RIT – rabbit infectivity test) – zcela experimentální metoda, která nemá pro klinickou praxi reálný diagnostický význam. Dříve se užívala k odlišení nevenerických treponematóz.
1.5. Molekulární diagnostika:
– PCR (polymerase chain reaction, polymerázová řetězová reakce) je amplifikační metoda pro průkaz specifických konzervativních úseků genomu. Využití PCR k přímému průkazu DNA TPP v suspektních lezích a v liquoru přináší téměř 100 % specificitu (treponemata, která se vyskytují v naší zeměpisné oblasti mají pouze 5 % homologii genomu s TPP). Citlivost testu je srovnatelná s RIT a blíží se 1 mikroorganismu/5 μl. Jako biologický materiál pro průkaz přítomnosti mikroba lze použít stěry z lézí, biopsii, plnou krev, CSF, tkáň, amniovou tekutinu, placentární trofoblastické klky, do parafinu zalité tkáně. Vzorek není nutné zpracovávat bezprostředně po odběru a je možné jej přepravovat bez zvláštních opatření, pokud je cílovou molekulou DNA. Stanovení přítomnosti TPP v CSF je specifické (není zkřížená reaktivita s borreliemi či jinými bakteriemi, případně viry) a má rozhodující vliv na prognózu onemocnění i strategii terapie.
V případě využití PCR lze při diagnostice syfilis congenita dosáhnout maximální možné spolehlivosti vyloučením interference s organizmem matky v důsledku pasivního přenosu protilátek. Multiplexní PCR umožňuje současný průkaz více původců (mikrobiálních i virových) genitálních lézí z jednoho vzorku.
Molekulárně biologických technologií, včetně PCR, lze použít i k průkazu příčiny rezistence TPP na antibiotika, např. makrolidy, tetracykliny.
NRL se zúčastnila grantového výzkumného úkolu zabývajícího se standardizací metodiky pro rutinní praxi a má tento superkonziliární test k dispozici.
– Přímá hybridizace je diagnostika pomocí vazby definovaného úseku genetického materiálu patogenu se specifickou značenou sondou, pro průkaz původce syfilis je většinou málo citlivá.
2. NEPŘÍMÁ LABORATORNÍ DIAGNOSTIKA
Průkaz protilátek v séru, plazmě nebo CSF. U imunokompetentního pacienta je možné nalézt protilátkovou odpověď na přítomnost treponemat sérologickými testy zhruba od 4. – 5. týdne po infekci a dále většinou během celého života ( a to i po úspěšné léčbě – tř. IgG). Je ovšem nutné posuzovat pacienta jako celek včetně anamnézy jak epidemiologické, tak i případně podaných antibiotik v inkubační době, která mohou ovlivnit sérokonverzi a být důvodem falešně negativních nálezů. Spolehlivost a reprodukovatelnost vyšetření protilátek v krvi a liquoru je důvodem jeho nezastupitelnosti při rutinní diagnostice.
2.1. Netreponemové testy, prokazující nespecifické antikardiolipinové protilátky (mikro- a makroflokulační metodiky), jsou využívány (v kombinaci s treponemovými testy) ke screeningu a k posouzení aktivity choroby a úspěšnosti léčby (vzestup, resp. pokles titru protilátek). Před zavedením prvního specifického testu (Nelson-Mayerova testu) byly jedinou možností ověření klinického a mikroskopického nálezu. Bordett-Wassermannova reakce „BWR“ se pak stala jakousi „obchodní značkou“ spojovanou s vyšetřením příjice a ačkoliv byla později nahrazena k uživatelům přátelštějšími metodami (RPR, VDRL apod.) a překonána treponemovými testy, zůstává pro běžného „člověka klinického“ tím nejsrozumitelnějším synonymem lues. Synonymem, které sdělí vše aniž by nezasvěcenému naznačilo jakou to chorobou pacient vlastně trpí.
Jsou však zatíženy poměrně vysokým procentem (2-10%) falešně pozitivních výsledků (Tabulka 1), dlouhodobě izolovaně pozitivní netreponemový test by měl být impulzem k detailnímu internímu vyšetření možných příčin (autoimunitní onem., maligní onem., antifosfolipidový syndrom apod.), a také výskytem falešně negativních reakcí (v počátku onemocnění před sérokonverzí; u pozdní latentní syfilis představuje až 30% případů; zonální fenomén u akutní syfilis). Zonální fenomén se může projevit u sér s vysokým titrem specifických a nespecifických protilátek v době akutní syfilis (1-2%) a znamená únik aktivních, infekčních onemocnění. V neředěném séru je výsledek vyšetření negativní, se stoupajícím ředěním dochází k rozvoji pozitivní reakce až do endpointu titrace. Vzhledem k uvedeným skutečnostem není vhodné používat netreponemové testy jako jediný screeningový test.
Tabulka 1: Příčiny falešně pozitivních výsledků v netreponemových testech.
| Akutní příčiny (trvání méně než 6 měsíců) | Chronické příčiny (trvání déle než 6 měsíců) |
| virové hepatitidy | hepatitidy |
| příušnice | příušnice |
| infekční mononukleóza | infekční mononukleóza |
| plané neštovice | plané neštovice |
| ostatní virové infekce | ostatní virové infekce |
| malárie | malárie |
| rozsáhlý infarkt myokardu | rozsáhlý infarkt myokardu |
| rozsáhlé poškození tkáně (popáleniny, crush sy) | |
| očkování | |
| gravidita | |
| užívání drog |
Protilátky jsou detekovatelné již cca 4 týdny po infekci.
VDRL (Veneral disease research laboratory) mikro test je mikroskopický netreponemový test vhodný k vyšetření séra i liquoru (dle WHO je jediným z netreponemových testů určeným pro standardní vyšetření liquoru). Má všechny přednosti i nedostatky své skupiny, včetně výskytu zonálního fenoménu.
RPR (Rapid plasma reagin) test – obdoba VDRL mikro testu s makroskopicky vizualizovanou reakcí (karbonové částice, pigmenty). Komerčně dostupné metodiky obvykle nevyžadují inaktivaci séra (na rozdíl od VDRL).
2.2. Treponemové testy jsou založeny na detekci specifických protilátek proti antigenům TPP (lipoproteinům). Patří k nim metody screeningového panelu (TPHA, TP-PA, EIA, ELISA, chemiluminiscence) i konfirmační postupy k ověření diagnózy. Je možno odděleně vyšetřovat IgM třídu protilátek (posouzení aktivity syfilis a úspěšnosti léčby, intrauterinní infekce). Samozřejmě i zde je nutné počítat s možným výskytem falešně negativních reakcí, zejména v inkubační době a na počátku I. stadia, ( cca 2% u testů pro třídu IgG a až 30% u testů pro třídu IgM) a falešně pozitivních (cca 1-2%) reakcí (Tabulka 2).
Tabulka 2: Příčiny falešně pozitivních reakcí v treponemových testech.
| Akutní příčiny (trvání méně než 6 měsíců) | Chronické příčiny (trvání déle než 6 měsíců) |
| hepatitidy | autoimunitní onemocnění |
| borrelióza | abnormality imunoglobulinů |
| infekční mononukleóza | nevenerické treponematózy |
| malárie | malignity |
| očkování | |
| užívání drog | |
| idiopatické |
Sérokonverzi jsou schopny zachytit okolo 5. – 6. týdne po infekci.
2.2.1. Screeningové treponemové testy – v průběhu vývoje od 60. let (hemaglutinace) až po současnost (EIA/ELISA, imunochromatografie, chemiluminiscence) se zvýšila jejich specificita a citlivost. Pozitivita přetrvává dlouhodobě i po úspěšné léčbě a je obrazem prodělané infekce. Protilátky zachycované těmito testy přestupují placentární bariéru (tř. IgG) a nejsou proto vhodné pro diagnostiku infekce plodu.
MHA-TP (Microhaemaglutinace Treponema pallidum) – obdoba dřívějšího zkumavkového TPHA testu (Treponema pallidum haemaglutinace) v mikrotitračních destičkách. Nosičem specifických antigenů jsou zvířecí krvinky. Pracuje s minimálním množstvím séra, plazmy nebo liquoru.
TP-PA (Treponema pallidum particule aglutination) – principiálně shodný test s MHA-TP. Nosičem specifických antigenů jsou namísto zvířecích krvinek inertní želatinové barevné částice, což přináší mimo jiné vyšší stabilitu vyrobených šarží testů.
ELISA a EIA (Enzyme imunolinked assay, enzyme imuno assay) – varianty total (pro všechny tř. protilátek současně) jsou vhodné ke screeningovému vyšetření séra, plazmy nebo liquoru. Vývoj přináší na trh stále citlivější diagnostika s odpovídající specificitou. Umožňují vyšetřování větších skupin vzorků a automatizaci. Vyhovují podmínkám správné laboratorní praxe a nutnosti dokumentovat každý procesní krok reakce.
Imunochromatografické testy – jsou určeny pro rychlou diagnostiku v urgentních případech nebo v terénních studiích s rizikem nižší citlivosti u počínajících a vyhasínajících onemocnění. Detekují přítomnost všech tříd protilátek společně vizualizovaných barevně v reakci se specifickými antigeny fixovanými v nitrocelulózové membráně.
Latex-aglutinační testy – stanoví přítomnost specifických protilátek bez rozlišení třídy aglutinací latexových částic nesoucích specifické antigeny TPP. Jsou rovněž určeny pro rychlé vyhledávací testování.
Chemiluniscenční testy (CLIA) – stanoví přítomnost protilátek odečtením kvanta světelné energie vyzářené po reakci konjugátu vázaného na specifické protilátky se startovací reagencií.Přinášejí výhodu automatizované, dokumentované diagnostiky z primární zkumavky s minimalizací možnosti lidské chyby a monitorováním procesu.
2.2.2. Konfirmační testy – slouží k ověření pozitivity vyhledávacích reakcí a potvrzení diagnózy. Skupina zahrnuje metody pro detekci protilátek ve třídě IgG a IgM ( IgM k posouzení aktivity onemocnění a úspěšnosti léčby).
FTA-ABS (fluorescenční-absorbční) IgG test – je považován za standardní konfirmační test s vysokou citlivostí (sérokonverze opakovaně dokumentována již ve 2. týdnu po infekci) a specificitou. Jako antigen pro vazbu protilátek využívá přímo usmrcené TPP kmene Nichols. Specifičnost reakce je zvýšena vysycením společných protilátek (např. s rody Borrelia, Leptospira a s ostatními zástupci rodu Treponema) sorbentem připraveným z Treponema phagedensis Reiter.
Westernblot IgG – umožní identifikaci protilátek proti jednotlivým hlavním antigenům TPP (získaným z virulentního kmene Nichols, obvykle lipoproteidů 15,5, 17 a 47 kDa) a tím i lepší posouzení vývoje onemocnění. Jednotlivé třídy protilátek se odlišují monospecifickými konjugáty.
Immunoline assay IgG – identifikace protilátek ve tř. IgG proti hlavním antigenům Treponema pallidum připraveným rekombinantně nebo semisynteticky.
TPI (Nelson-Mayerův Treponema pallidum imobilizační test) – první specifický test uvedený do praxe na konci 40.let 20.století. Protilátky (imobiliziny, které za účasti komplementu způsobují imobilizaci a následný rozpad buněk TPP) se objevují na přelomu primárního a sekundárního stadia syfilis. Původně byl považován za doživotní marker kontaktu s infekcí. Během let praxe a ve srovnání s ostatními specifickými testy se však ukázalo, že dochází po delší době ke spontánní negativizaci (vymizení imobilizinů) i u pacientů s neléčeným onemocněním. Přesto, že je zatížen pouze malým procentem falešně pozitivních reakcí, nároky na provedení testu (vybavení laboratoře, dostupnost živého virulentního kmene TPP, vyškolený personál) odsouvají metodiku mezi superkonzliární konfirmační vyšetření.
FTA-ABS IgM – využívá konjugát proti lidským IgM protilátkám. Vzhledem ke kompetici IgG a IgM protilátek o antigenní determinanty TPP v průběhu reakce je jeho citlivost menší.
19S IgM FTA-ABS – vzhledem k nutné předchozí separaci IgM frakce séra je tento specifický a citlivý test určen spíše pro experimentální práci.
19S IgM SPHA (19S IgM Solid phase haemadsorbtion) – test je založený na principu capture (vychytání) IgM protilátek z vyšetřovaného materiálu před vizualizací (nosičem specifických antigenů jsou zvířecí krvinky nebo syntetické mikropartikule). Tento princip zvyšuje citlivost metodiky. Dále je možné určení titru protilátek a jeho následné sledování v průběhu dispenzární péče.
ELISA IgM – moderní testy řeší řadu úskalí vyšetření protilátek IgM třídy a postupně se stávají citlivějšími a specifičtějšími. Uplatní se při posuzování aktivity onemocnění a odlišení syfilis congenita.
Westernblot IgM – umožní identifikaci protilátek v dané třídě proti jednotlivým hlavním antigenům TPP a tím i lepší posouzení vývoje onemocnění.
ZÁVĚR
I přes rozsáhlou škálu klasických přímých i nepřímých testů, vhodných pro diagnostiku syfilis, zůstává řada situací, ve kterých mohou být výsledky vyšetření problematické a neumožňují rychlé a spolehlivé stanovení diagnózy, jedná se zejména o:
Syfilis congenita – laboratorní diagnostika se v současné době rutinně opírá pouze o průkaz IgM protilátek, které nepronikají přes placentární bariéru (na rozdíl od IgG), přímé testy běžně využívány nejsou. Zhodnocení sérologie je však zatíženo řadou fyziologických i patologických jevů, umožňujících definitivní sérologické stanovení diagnózy až po 18. měsíci věku (úplné vymizení přenesených protilátek).U novorozence je tedy diagnóza stanovena vždy na základě anamnézy matky, klinického stavu dítěte a nálezu protilátek v séru. Nadějné je provedení PCR.
Neurosyfilis – obtížné odlišení intrathekální produkce imunoglobulinů, nutnost posoudit porušení haematoencephalické bariery (naprosto nezbytný je současný odběr krve spolu s liquorem).
Posouzení infekčního rizika – žádný z přímých testů není schopen spolehlivě detekovat přítomnost treponemat v krvi (vzhledem k malému množství bakterií a poměrně krátké a individuální bakteriémii). Protilátky (IgM) mohou pouze naznačit aktivitu procesu.
Nemožnost kultivovat TPP in vitro je významným nedostatkem při objektivním průkazu syfilis. S rozvojem molekulární biologie a diagnostiky se nabízí nové možnosti. Standardní test odpovídající správné laboratorní praxi (včetně vnitřní kontroly falešně negativních výsledků) vhodně doplní sérologické testy, které v diagnostice syfilis mají klíčovou a nezastupitelnou roli. PCR lze použít k typizaci kmenů (epidemiologie syfilis a nevenerických treponematóz) na základě specifických sekvencí, ale i ke kvantifikaci mikroorganizmů, dále k rozlišení živých a mrtvých buněk a k průkazu DNA TPP v biologických archivních materiálech atd.
Zásadním aspektem diagnostiky syfilis je nutná mezioborová spolupráce. Definitivní diagnózu může stanovit pouze klinický lékař na základě anamnézy, klinických projevů a laboratorního vyšetření, které je ovšem nezastupitelné.
Legenda obrázků:
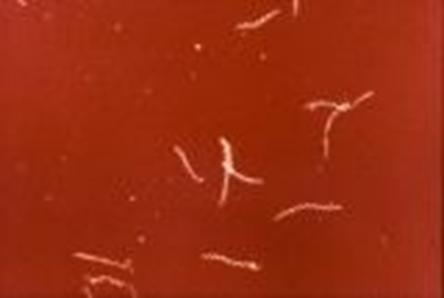
Obrázek 1: Obrázek 1: Treponema pallidum subsp. pallidum – nepřímá imunofluorescence (foto: MUDr. Magdalena Knappová, NRL pro diagnostiku syfilis 1986)
Literatura:
1. CDC.Sexually Transmitted Diseases treatment guidelines. Morbidity and mortality weekly report, 2006, 55, 100p.
2. Radolf, J.D., Lukehart, S.A. Pathogenic Treponema. Caister Academic press.England. 2006 ISBN: 1-904455-10-7
3. Votava, M., et al. Lékařská mikrobiologie speciální. Brno: Neptun, 2003, 495 p. ISBN 80-902896-6-5
4. Zákoucká H. Syfilis – tradiční choroba, současný problém I. Zprávy CEM (SZÚ, Praha) 2007; 16(9): 422-426.
MUDr. Hana Zákoucká
NRL pro syfilis, SZÚ – CEM, Praha






